Катализаторы крекинга
Катализаторы современных крупнотоннажных процессов каталитического крекинга, осуществляемых при высоких температурахт(500…800 °С) в режиме интенсивного массо- и теплообмена в аппаратах с движущимся или псевдоожиженным слоем катализатора, должны обладать не только высокими активностью, селективностью и термостабильностью, но и удовлетворять повышенным требованиям к ним по регенерационным, механическим и некоторым другим эксплуатационным свойствам. Промышленные катализаторы крекинга представляют собой в этой связи сложные многокомпонентные системы, состоящие:
- из матрицы (носителя);
- активного компонента — цеолита;
- вспомогательных активных и неактивных добавок.
Матрица катализаторов крекинга выполняет функции как носителя — поверхности, на которой затем диспергируют основной активный компонент — цеолит и вспомогательные добавки, так и слабого кислотного катализатора предварительного (первичного) крекирования высокомолекулярного исходного нефтяного сырья. В качестве материала матрицы современных катализаторов крекинга преимущественно применяют синтетический аморфный алюмосиликат с высокой удельной поверхностью и оптимальной поровой структурой, обеспечивающей доступ для крупных молекул крекируемого сырья.
Аморфные алюмосиликаты являлись основными промышленными катализаторами крекинга до разработки цеолитсодержащих катализаторов. Синтезируются они при взаимодействии растворов, содержащих оксиды алюминия и кремния, например жидкого стекла Na2O · 3SiO2 и сернокислого алюминия Al2(SO4)3. Химический состав аморфного алюмосиликата может быть выражен формулой Na2O(Al2O3 · xSiО2) где х — число молей SiO2 на 1 моль Al2O3. Обычно в промышленных аморфных алюмосиликатах содержание оксида алюминия находится в пределах 6…30 % мас.
Аморфные алюмосиликаты обладают ионообменными свойствами, а для придания каталитической активности обрабатывают их раствором сернокислого алюминия для замещения катионов Na+ на Аl3+. Высушенные и прокаленные аморфные алюмосиликаты проявляют протонную и апротонную кислотности. При этом по мере повышения температуры прокаливания происходит превращение протонных кислотных центров в апротонные.
Активным компонентом катализаторов крекинга является цеолит, который позволяет осуществлять вторичные каталитические превращения углеводородов сырья с образованием конечных целевых продуктов.
Цеолиты (от греч. цео — кипящий, литос — камень) представляют собой алюмосиликаты с трехмерной кристаллической структурой следующей общей формулы:
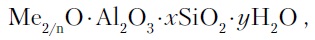
где n — валентность катиона металла Me; х — мольное соотношение оксидов кремния и алюминия, называемое силикатным модулем; у — число молей воды.
В настоящее время насчитывается несколько десятков разновидностей природных и синтетических цеолитов, отличающихся структурой, типом катионов Me, силикатным модулем и числом молекул кристаллизационной воды. Структура цеолитов характеризуется наличием большого числа полостей, соединенных между собой окнами, или микроканалами, размеры которых сравнимы с размерами реагирующих молекул. Обычно полости имеют больший диаметр, чем каналы (или окна). Например, в цеолите типа шабазит имеется 3 · 1020 полостей диаметром 11,4 Å, в каждую полость которого может поместиться 24 молекулы воды. Диаметр окон шабазита составляет 4,9 Å. При нагреве цеолита вода удаляется и образуется ячеистая структура. Удельная поверхность цеолитов достигает 700…1000 м/г. Обезвоженные цеолиты способны избирательно адсорбировать молекулы различных веществ в зависимости от размеров каналов. Разумеется, если диаметр адсорбируемого вещества больше, чем сечение канала, то оно не может проникнуть во внутренние поры цеолита (ситовой эффект). Так, при диаметре канала (окна) 4 Å цеолит не может адсорбировать углеводороды нормального строения, диаметр молекул которых равен = 4,9 Å.
Обычно тип структуры синтетического цеолита обозначают буквами латинского алфавита А, X, Y, ... L и т. д. Перед буквами ставят химическую формулу катиона металла, компенсирующего отрицательный заряд алюминия в алюмосиликате. Например, СаХ означает цеолит типа X в кальциевой обменной форме; LaY, ReY — соответственно лантановая и редкоземельная форма цеолита Y.
Принято подразделять цеолиты в зависимости от величины силикатного модуля х на следующие структурные типы:

За рубежом цеолиты классифицируют иначе: перед буквой, обозначающей тип цеолита, ставят цифру, соответствующую максимальному диаметру молекул (в ангстремах), адсорбируемых данным цеолитом.
По этой классификации цеолиту NaA соответствует цеолит 4А, цеолиту СаА — 5А, цеолиту NaX — 13Х, цеолиту СаХ — 10Х и т. д.
Ниже приводим размеры полостей и окон для некоторых синтетических цеолитов:
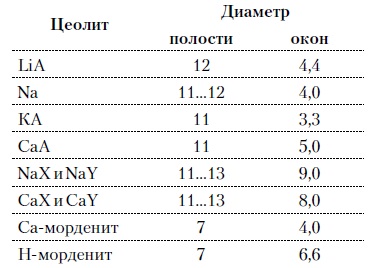
Цеолиты типа А, имеющие малые размеры окон (3,3…5 Å) и небольшой силикатный модуль (1,8…2,0), как правило, не используются в каталитических процессах и применяются в качестве адсорбентов. В каталитических процессах, в том числе крекинга нефтяного сырья, наибольшее применение нашли цеолиты типа X и Y — оба аналоги природного фожазита. В последние годы широкое распространение получают высококремнеземные трубчатые цеолиты L с силикатным модулем более 30 (например, ZSM).
Первичной основой (структурной единицей) кристаллической решетки цеолитов X и Y является тетраэдр, состоящий из четырех анионов кислорода, которые окружены значительно меньшими по размерам ионами кремния или алюминия (рис. 6.2а). 24 тетраэдра образуют вторичную структурную единицу — усеченный октаэдр (кубооктаэдр, который содержит восемь шестиугольных и шесть квадратных поверхностей), так называемую содалитовую клетку (рис. 6.2б). На следующей ступени структурирования четыре кубооктаэдра объединяются в тетраэдрическую конфигурацию вокруг пятого при помощи шестиугольных призм, образуя суперклетку (рис. 6.2в). В результате объединения множества суперклеток (в фожазите их восемь) в регулярную систему формируется элементарная ячейка цеолита (рис. 6.2г).
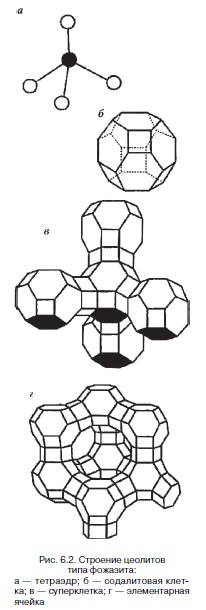
Тетраэдры из оксидов кремния и алюминия расположены так, что цеолиты имеют открытые участки структуры. Это и создает систему пор с высокой удельной поверхностью. Химическую формулу первичной структурной единицы — тетраэдров кремния и алюминия — можно представить в виде:
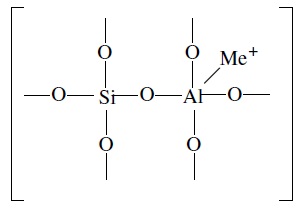
Тетраэдры с ионами Si4+ электрически нейтральны, а тетраэдры с ионами трехвалентного алюминия Аl3+ имеют заряд минус единица, который нейтрализуется положительным зарядом катиона Ме+ (сначала катионом Na+, поскольку синтез чаще ведется в щелочной среде, затем в результате катионного обмена — катионами других металлов, катионом NH4 или протоном Н+).
Наличие заряженных ионов алюминия на поверхности цеолита (центры Бренстеда) и обусловливает кислотные свойства и, следовательно, его каталитическую активность.
Натриевая форма цеолитов каталитически малоактивна и наименее термостабильна. Оба эти показателя существенно улучшаются при увеличении силикатного модуля цеолитов, а также степени ионного обмена на двухвалентные и особенно на трехвалентные металлы. Среди них более термостабильны цеолиты типа ReY, обладающие к тому же важным свойством — высокой каталитической активностью. Благодаря этим достоинствам цеолиты серии ReY как активный компонент катализаторов крекинга получили исключительно широкое применение в мировой нефтепереработке.
Важным этапом в области дальнейшего совершенствования цеолитных катализаторов крекинга явилась разработка (в 1985 г. фирмой «Юнион карбаид») нового поколения цеолитов, не содержащих редкоземельных элементов, — так называемых химически стабилизированных цеолитов.
В условиях воздействия высоких температур и водяного пара цеолиты ReY даже при полном редкоземельном обмене подвергаются частичной деалюминации:
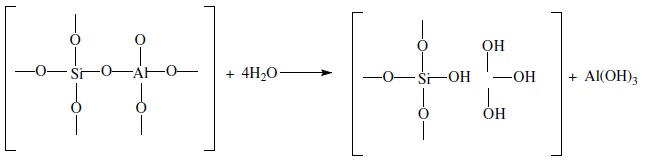
В результате гидродеалюминации в суперклетке образуется пустота, что является причиной постепенного разрушения кристалла цеолита. Гидроксид алюминия, который не выводится из кристалла, а откладывается внутри суперклетки цеолита, обладает, кроме того, нежелательной каталитической активностью (кислотностью Льюиса, ускоряющей реакции образования легких газов и кокса).
Химическая стабилизация цеолитов заключается в низкотемпературной химической обработке их фторосиликатом аммония по реакции:
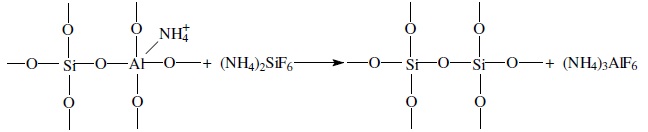
В результате обмена ионов Аl на ионы Si образуется более прочный и термостабильный цеолит с повышенным силикатным модулем и кристаллической решеткой без пустот. Еще одно достоинство этого
процесса, обозначенного как процесс LS-210, — это то, что фтороалюминат аммония растворим и полностью выводится из кристаллической решетки цеолита. Цеолиты LS-210 (торговые марки Альфа, Бета, Эпсилон и Омега) характеризуются повышенной гидротермической стабильностью и селективностью, повышенной стабильностью по отношению к дезактивации металлами, но пониженной активностью в реакциях переноса водорода, что способствует повышению выхода изоолефинов в газах крекинга и октановых чисел бензинов.
Недостатком всех цеолитов является их не очень высокая механическая прочность в чистом виде, и потому они в качестве промышленного катализатора не используются. Обычно их вводят в диспергированном виде в матрицу катализаторов в количестве 10…20 % мас.
Вспомогательные добавки улучшают или придают некоторые специфические физико-химические и механические свойства цеолитсодержащим алюмосиликатным катализаторам (ЦСК) крекинга. ЦСК без вспомогательных добавок не могут полностью удовлетворять всему комплексу требований, предъявляемых к современным промышленным катализаторам крекинга. Так, матрица и активный компонент — цеолит, входящий в состав ЦСК, обладают только кислотной активностью, в то время как для организации интенсивной регенерации закоксованного катализатора требуется наличие металлических центров, катализирующих реакции окислительно-восстановительного типа. Современные и перспективные процессы каталитического крекинга требуют улучшения и оптимизации дополнительно таких свойств ЦСК, как износостойкость, механическая прочность, текучесть, стойкость к отравляющему воздействию металлов сырья и т. д., а также тех свойств, которые обеспечивают экологическую чистоту газовых выбросов в атмосферу.
Ниже приводится перечень наиболее типичных вспомогательных добавок:
- в качестве промоторов, интенсифицирующих регенерацию закоксованного катализатора, применяют чаще всего платину, нанесенную в малых концентрациях (< 0,1 % мас.) непосредственно на ЦСК или на окись алюминия с использованием как самостоятельной добавки к ЦСК. Применение промоторов окисления на основе Pt позволяет значительно повысить полноту и скорость сгорания кокса катализатораи, что не менее важно, существенно понизить содержание монооксида углерода в газах регенерации, тем самым предотвратить неконтролируемое загорание СО над слоем катализатора в регенераторе, приводящее к прогару циклонов, котлов-утилизаторов и другого оборудования(из отечественных промоторов окисления можно отметить КО-4, КО-9, Оксипром-1 и Оксипром-2);
- с целью улучшения качества целевых продуктов в последние годы стали применять добавки на основе ZSM-5, повышающие октановое число бензинов на 1…2 пункта;
- для снижения дезактивирующего влияния примесей сырья наЦСК в последние годы весьма эффективно применяют технологию каталитического крекинга с подачей в сырье специальных пассиваторов металлов, представляющих собой металлоорганические комплексы сурьмы, висмута, фосфора или олова. Сущность эффекта пассивациизаключается в переводе металлов, осадившихся на катализаторе, в неактивное (пассивное) состояние, например, в результате образования соединения типа шпинели. Пассивирующий агент вводят в сырье в виде водо- или маслорастворимой добавки. Подача пассиваторов резко снижает выход кокса и водорода, увеличивает выход бензина и производительность установки (в настоящее время пассиваторы применяют на 80 % установок каталитического крекинга остатков в США и около 50 % установок в Западной Европе). В последние годы внедряется ЦСК с твердой добавкой — ловушкой ванадия и никеля, содержащей оксиды Са, Mg, титанат бария и др., адсорбирующие в 6...10 раз больше металлов, чем сам катализатор;
- при каталитическом крекинге негидроочищенного сырья образуются (в регенераторе) оксиды серы и азота, отравляющие атмосферу. В связи с возросшими требованиями к экологической безопасности промышленных процессов исключительно актуальной становится проблема улавливания вредных компонентов газовых выбросов. Если в состав ЦСК ввести твердую добавку MgO или СаО, то такой катализатор становится переносчиком оксидов серы из регенератора в реактор по схеме:
в регенераторе: MgO + SO3 → MgSO4 ;
в реакторе: MgSO4 + 4Н2 → MgO + H2S + 3H2O ;
или 2MgSO4 + СН4 → 2MgO + 2H2S + СО2 .
Образующийся сероводород, выводимый из реактора вместе с продуктами крекинга, будет извлекаться затем из газов аминной очисткой;
- для повышения механической прочности ЦСК в состав аморфной матрицы дополнительно вводят тонкодисперсную окись алюминия (α-форму). Кроме того, для снижения потерь катализатора от испарения и уменьшения коррозии аппаратуры в системах катализатора в циркулирующий катализатор вводят смазывающие порошки из смеси окиси магния, карбоната и фосфата кальция, иногда титаната бария. Эти добавки взаимодействуют при высокой температуре с поверхностью катализатора, в результате чего на ней образуется глянец, способствующий снижению истирания.
Промышленные катализаторы крекинга. На отечественных установках с движущимся слоем шарикового катализатора применялись и продолжают пока применяться шариковые катализаторы АШНЦ-3 (без РЗЭ), АШНЦ-6, Цеокар-2 и Цеокар-4 (все с РЗЭ).
Из микросферических ЦСК применение находят: КМЦР-2 (2 % La2O3), МЦ-5 и РСГ-6Ц (по 4 % La2O3), КМЦР-4 (с промотором дожига) и др. Из зарубежных ЦСК более известны следующие марки катализаторов: Дюрабед (5, 6, 8, 9), Супер (Д, экстра Д), (1–7), CBZ (1–4), Октакэт-11, Резидкэт (20, 30) и другие.
Мировое производство катализаторов крекинга в настоящее время составляет около 400 тыс. т в год. По объему производства наиболее крупными катализаторными фабриками владеют фирмы «Грейс Девисон» (США, Германия — 43 %), «Энгельгард» (США, Нидерланды — 27 %) и «Акзо Нобель» (США, Нидерланды, Бразилия — 26 %).
Подавляющую часть катализаторов крекинга производят по традиционной технологии «со связующим», используя в стадии нанесения синтезированного цеолита на поверхность носителя (алюмосиликата) связующий компонент. Затем осуществляют стадии распылительной сушки, ионного обмена термохимической обработкой, нанесения промоторов, вспомогательных добавок, прокалки, компаундирования и т. д.
В последние годы было разработано и широко внедряется новое исключительно эффективное поколение так называемых катализаторов крекинга «без связующего» фирмы «Энгельгард» (например, марки Д8Р-840). По этой технологии синтез цеолита осуществляется непосредственно в порах носителя без использования связующего компонента. Характерная особенность этих катализаторов — весьма высокая их насыпная масса (0,92…0,96 г/мл), что обеспечивает высокую эффективную работу циклонов, устойчивое и стабильное псевдоожижение, устойчивую регулируемую скорость циркуляции и перенос большого количества тепла из регенератора в реактор. Надо отметить также следующие достоинства катализаторов фирмы «Энгельгард»:
- высокие активность и термопаровая стабильность;
- высокие механическая прочность и износостойкость;
- больший выход бензина (53 вместо 49 % у Супер Д) при более высоком октановом числе (92 против 87) и меньшем выходе кокса;
- меньший удельный расход (0,27 вместо 0,34 кг/г).
ТЕХНОЛОГИЯ И ОБОРУДОВАНИЕ ПРОЦЕССОВ ПЕРЕРАБОТКИ НЕФТИ И ГАЗА, С. А. Ахметов, Т. П. Сериков, И. Р. Кузеев, М. И. Баязитов, 2006
